PRÍRUČKA PRE DÁVKOVANIE A PODÁVANIE Tento liek je predmetom ďalšieho monitorovania. Vyžaduje sa špeciálne podávanie hlásení v súvislosti s nežiaducimi
|
|
|
- Egon Daněk
- pred 4 rokmi
- Prehliadani:
Prepis
1 PRÍRUČKA PRE DÁVKOVANIE A PODÁVANIE Tento liek je predmetom ďalšieho monitorovania. Vyžaduje sa špeciálne podávanie hlásení v súvislosti s nežiaducimi reakciami. Skrátené informácie o predpisovaní nájdete na strane 8.
2 PRÍRUČKA PRE DÁVKOVANIE A PODÁVANIE Príprava na podanie lieku BRINEURA 1 Brineura je indikovaná na liečbu ochorenia neuronálna ceroidná lipofuscinóza typu 2 (CLN2), známeho aj ako deficit tripeptidylpeptidázy 1 (TPP1). Nasledujúce kroky sa odporúčajú pre dávkovanie a podávanie lieku BRINEURA a vychádzajú zo súhrnu charakteristických vlastností lieku. Ďalšie informácie a pokyny nájdete v úplnom znení súhrnu charakteristických vlastností lieku, v pokynoch vášho lekára a predpisoch a postupoch vášho zdravotníckeho zariadenia. BRINEURA sa smie podávať len intracerebroventrikulárnou cestou. BRINEURA smie podávať len vyškolený zdravotnícky pracovník s poznatkami o intracerebroventrikulárnom podávaní v zdravotníckom zariadení. Osobitné upozornenia a opatrenia pri používaní 1 Komplikácie súvisiace so zariadením BRINEURA sa musí podávať aseptickým postupom, aby sa znížilo riziko infekcie. V klinických štúdiách sa pozorovali prípady infekcií súvisiacich so zariadením na intracerebroventrikulárny prístup. V týchto prípadoch sa podali antibiotiká, zariadenie na intracerebroventrikulárny prístup sa vymenilo a pokračovalo sa v liečbe liekom BRINEURA. Zdravotnícki pracovníci majú pred každou infúziou skontrolovať celistvosť kože pokožky hlavy, aby sa uistili, že zariadenie na intracerebroventrikulárny prístup je neporušené. Pred začatím infúzie lieku BRINEURA sa musí vykonať kontrola miesta podania infúzie a kontrola priechodnosti, aby sa zistilo prípadné unikanie tekutiny zo zariadenia na intracerebroventrikulárny prístup a/alebo jeho porucha. Na potvrdenie neporušenosti zariadenia môže byť potrebná konzultácia s neurochirurgom. Liečba liekom BRINEURA sa má v prípade poruchy zariadenia prerušiť a pred ďalšími infúziami bude možno potrebné zariadenie na prístup vymeniť. V prípade komplikácií súvisiacich so zariadením na intracerebroventrikulárny prístup nájdete ďalšie pokyny na označení obalu zariadenia od výrobcu. Opatrnosť je potrebná u pacientov náchylných na komplikácie v dôsledku podávania intracerebroventrikulárneho lieku vrátane pacientov s obštrukčným hydrocefalom. Klinické a laboratórne monitorovanie Pred začiatkom podávania infúzie v zdravotníckom zariadení, pravidelne počas nej i po nej sa majú monitorovať životné funkcie. Po skončení infúzie sa má klinicky vyhodnotiť stav pacienta, pričom ak je to klinicky indikované, môže byť potrebné dlhodobejšie sledovanie, najmä u pacientov mladších ako 3 roky. Pacienti s bradykardiou, poruchou vedenia srdcových vzruchov alebo so štrukturálnym ochorením srdca v anamnéze sa majú počas infúzie monitorovať pomocou elektrokardiogramu (EKG), pretože u niektorých pacientov s ochorením CLN2 sa môžu rozvinúť poruchy vedenia srdcových vzruchov alebo ochorenie srdca. U pacientov s normálnou funkciou srdca sa má každých 6 mesiacov vykonať vyšetrenie pomocou 12-zvodového EKG. Vzorky cerebrospinálneho moku (CSF) sa majú pravidelne posielať na testovanie výskytu subklinických infekcií súvisiacich so zariadením. Pediatrická populácia Do klinických skúšaní neboli zaradení žiadni pacienti s pokročilou progresiou ochorenia na začiatku liečby a nie sú k dispozícii žiadne klinické údaje o deťoch vo veku < 2 roky. Pacienti s pokročilým ochorením CLN2 a novorodenci môžu mať zníženú celistvosť hematoencefalickej bariéry. Účinky potenciálne zvýšenej expozície lieku na periférny systém nie sú známe. Obsah sodíka Tento liek obsahuje 44 mg sodíka na injekčnú liekovku lieku BRINEURA a preplachovacieho roztoku. To treba vziať do úvahy u pacientov na diéte s kontrolovaným obsahom sodíka. Odporúčaná dávka 1 BRINEURA 150 mg infúzny roztok je dostupný v jednorazových injekčných liekovkách obsahujúcich 5 ml roztoku. Každý ml infúzneho roztoku obsahuje 30 mg cerliponázy alfa. 2
3 Odporúčaná dávka je 300 mg (celkovo 10 ml z dvoch liekoviek), ktorá sa podáva jedenkrát za dva týždne intracerebroventrikulárnou infúziou. U pacientov mladších ako 2 roky sa odporúčajú nižšie dávky. 30 až 60 minút pred začiatkom infúzie sa odporúča premedikácia pacientov antihistaminikami s antipyretikami alebo bez nich. Pediatrická populácia Bezpečnosť a účinnosť lieku BRINEURA u detí vo veku menej ako 3 roky neboli doteraz stanovené. K dispozícii sú obmedzené údaje o deťoch vo veku 2 roky a nie sú k dispozícii žiadne klinické údaje o deťoch mladších ako 2 roky. Dávkovanie je založené na veku pacientov v čase liečby. U pacientov mladších ako 3 roky odporúčaná dávka zodpovedá dávkovaniu použitému v prebiehajúcej klinickej štúdii. BRINEURA sa má podávať podľa nasledujúcej odporúčanej dávky jedenkrát za dva týždne: Od narodenia do < 6 mesiacov: 100 mg 6 mesiacov až < 1 rok: 150 mg 1 rok až < 2 roky: 200 mg (prvé 4 dávky), 300 mg (nasledujúce dávky) 2 roky: 300 mg Úprava dávky Úpravy dávky budú možno potrebné u pacientov, ktorí netolerujú infúziu. Dávku možno znížiť o 50 % a/alebo je možné znížiť rýchlosť podávania infúzie. Ak sa infúzia preruší v dôsledku reakcie z precitlivenosti, má sa znova začať na úrovni približne jednej polovice pôvodnej rýchlosti podávania infúzie, pri ktorej došlo k reakcii z precitlivenosti. Infúzia sa má prerušiť a/alebo rýchlosť podávania sa má znížiť u pacientov, u ktorých podľa úsudku ošetrujúceho lekára môže počas infúzie dôjsť k zvýšeniu intrakraniálneho tlaku, čomu nasvedčujú príznaky ako bolesť hlavy, nauzea, vracanie alebo zhoršený psychický stav. Tieto opatrenia sú mimoriadne dôležité u pacientov vo veku menej ako 3 roky. Uchovávanie a starostlivosť 1 Jedna škatuľa lieku BRINEURA obsahuje tri injekčné liekovky (dve injekčné liekovky BRINEURA a jednu injekčnú liekovku preplachovacieho roztoku). Každá injekčná liekovka lieku BRINEURA a preplachovacieho roztoku je určená len na jednorazové použitie: Uchovávajte vo zvislej polohe v mrazničke ( 25 C až 15 C). Uchovávajte v pôvodnom obale na ochranu pred svetlom. Neotvorené zmrazené injekčné liekovky majú čas použiteľnosti až 2 roky, pozri dátum exspirácie na škatuli. Pred použitím: Injekčné liekovky sa majú rozmraziť pri izbovej teplote počas približne 60 minút. Odporúča sa rozmrazovať injekčné liekovky mimo škatule. Počas rozmrazovania sa objaví kondenzácia. Injekčné liekovky nerozmrazujte ani neohrievajte žiadnym iným spôsobom. Injekčnými liekovkami netraste. BRINEURA a preplachovací roztok sa musia úplne rozmraziť a ihneď použiť. Liek sa má odobrať z neotvorených injekčných liekoviek až bezprostredne pred použitím. Ak okamžité použitie nie je možné, neotvorené injekčné liekovky lieku BRINEURA alebo preplachovacieho roztoku sa majú uchovávať pri teplote 2 8 C a použiť do 24 hodín. Ak sa otvorené liekovky alebo lieky natiahnuté v striekačkách nepoužijú ihneď, za podmienky a čas uchovávania pred použitím je zodpovedný používateľ. Nerieďte ani nemiešajte liek BRINEURA s inými liekmi. Nezmrazujte opakovane injekčné liekovky ani nezmrazujte striekačky s obsahom lieku BRINEURA alebo preplachovacieho roztoku. 3
4 PRÍRUČKA PRE DÁVKOVANIE A PODÁVANIE Pred podaním Pri príprave a podávaní je nutné prísne dodržiavať aseptické postupy. BRINEURA a preplachovací roztok sa smú podávať len intracerebroventrikulárnou cestou. Zariadenie na intracerebroventrikulárny prístup (zásobník a katéter) sa musí chirurgicky implantovať pred prvou infúziou. Implantované zariadenie na intracerebroventrikulárny prístup má byť vhodné na vytvorenie prístupu do mozgových komôr na účely terapeutického podávania. Potrebné sú nasledujúce infúzne komponenty (ale nedodávajú sa). Všetky infúzne komponenty musia byť sterilné a kompatibilné s liekom BRINEURA a preplachovacím roztokom: Zoznam kompatibilných infúznych komponentov nájdete v súhrne charakteristických vlastností lieku BRINEURA. Programovateľný lineárny dávkovač s príslušným rozsahom podávania, presnosťou rýchlosti podávania a alarmami pri nesprávnom podávaní alebo upchaní. Dávkovač musí byť možné naprogramovať tak, aby sa liek podával konštantnou rýchlosťou 2,5 ml/hod. Celkový čas podávania infúzie vrátanie lieku BRINEURA a potrebného preplachovacieho roztoku je približne 2 až 4,5 hodín, v závislosti od podávanej dávky a objemu. Dve jednorazové injekčné striekačky kompatibilné s vybavením dávkovača. Odporúčajú sa striekačky s objemom 10 až 20 ml. Dve jednorazové hypodermické injekčné ihly (21 G, 25,4 mm). Jedna jednorazová infúzna súprava. V prípade potreby možno pridať predlžovaciu hadičku. Odporúča sa dĺžka 150 až 206 cm (nie viac ako 400 cm) a vnútorný priemer 0,1 cm. 0,2 μm líniový filter. Líniový filter môže byť zabudovaný v infúznej súprave. Líniový filter sa má umiestniť čo najbližšie ako je to prakticky možné k vstupnej ihle. Neprerezávajúca vstupná ihla veľkosti 22 G alebo menšia s odporúčanou dĺžkou 16 mm. Riaďte sa odporúčaním výrobcu zariadenia na intracerebroventrikulárny prístup v súvislosti so vstupnou ihlou. Jedna prázdna sterilná jednorazová injekčná striekačka (na odber cerebrospinálneho moku (CSF) na kontrolu priechodnosti). Predlžovacia hadička Infúzna súprava s 0,2-mikrónovým líniovým filtrom vstupná ihla LEN NA I.C.V. INFÚZIU Striekačka zásobník katéter Pomôcka na I.C.V prístup Lineárny dávkovač Obrázok 1: Zostavenie infúzneho systému 4
5 Príprava lieku BRINEURA a preplachovacieho roztoku Škatuľu s dvomi injekčnými liekovkami lieku BRINEURA a s injekčnou liekovkou preplachovacieho roztoku vyberte z mrazničky: Injekčné liekovky sa majú rozmraziť pri izbovej teplote počas približne 60 minút. Odporúča sa rozmrazovať injekčné liekovky mimo škatule. Počas rozmrazovania sa objaví kondenzácia. Injekčné liekovky nerozmrazujte ani neohrievajte žiadnym iným spôsobom. Injekčnými liekovkami netraste. BRINEURA a preplachovací roztok sa musia úplne rozmraziť a ihneď použiť. Liek sa má odobrať z neotvorených injekčných liekoviek až bezprostredne pred použitím. Ak okamžité použitie nie je možné, neotvorené injekčné liekovky lieku BRINEURA alebo preplachovacieho roztoku sa majú uchovávať pri teplote 2 8 C a použiť do 24 hodín. Skontrolujte všetky rozmrazené injekčné liekovky: BRINEURA a preplachovací roztok majú byť číre až mierne opaleskujúce, bezfarebné až svetložlté. Injekčné liekovky BRINEURA môžu niekedy obsahovať tenké priesvitné vlákna alebo nepriehľadné častice. Tieto prirodzene sa vyskytujúce častice sú cerliponáza alfa. Tieto častice sa odstránia pomocou 0,2 μm líniového filtra bez toho, aby to malo zistiteľný vplyv na čistotu alebo silu lieku BRINEURA. Preplachovací roztok môže obsahovať častice, ktoré sa po úplnom rozmrazení injekčnej liekovky rozpustia. Nepoužívajte roztoky ak zmenili zafarbenie alebo ak sa v nich nachádzajú iné cudzorodé tuhé častice. ODOBRATIE LIEKU BRINEURA : Označte jednu nepoužitú sterilnú injekčnú striekačku nápisom Brineura a pripojte injekčnú ihlu. Snímte zelené snímateľné viečka z oboch injekčných liekoviek BRINEURA. S použitím aseptického postupu odoberte objem roztoku BRINEURA zodpovedajúci požadovanej dávke do sterilnej injekčnej striekačky označenej nápisom Brineura. Nerieďte liek BRINEURA. Nemiešajte liek BRINEURA so žiadnym iným liekom. Ihlu a prázdne injekčné liekovky zlikvidujte v súlade s národnými požiadavkami. ODOBRATIE PREPLACHOVACIEHO ROZTOKU: Stanovte objem preplachovacieho roztoku potrebného na zabezpečenie podania celého množstva lieku BRINEURA do mozgových komôr. Preplachovací objem vypočítate tak, že pripočítate plniaci objem všetkých infúznych komponentov vrátane zariadenia na intracerebroventrikulárny prístup. Označte jednu nepoužitú sterilnú injekčnú striekačku nápisom preplachovací roztok a pripojte injekčnú ihlu. Snímte žlté snímateľné viečko z injekčnej liekovky preplachovacieho roztoku. S použitím aseptického postupu odoberte príslušné množstvo preplachovacieho roztoku z injekčnej liekovky do novej sterilnej injekčnej striekačky označenej nápisom preplachovací roztok. Ihlu a injekčnú liekovku so zvyšným roztokom zlikvidujte. 5
6 PRÍRUČKA PRE DÁVKOVANIE A PODÁVANIE Podávanie lieku BRINEURA INTRACEREBROVENTRIKULÁRNA INFÚZIA LIEKU BRINEURA : LLiek BRINEURA podajte pred preplachovacím roztokom. 1 Infúznu hadičku označte nápisom Len na intracerebroventrikulárnu infúziu. 2 Ak používate predlžovaciu hadičku, pripojte k nej injekčnú striekačku obsahujúcu liek BRINEURA inak pripojte injekčnú striekačku k infúznej súprave. Infúzna súprava musí byť vybavená 0,2 µm líniovým filtrom. Pozri obrázok 1. 3 Naplňte infúzne komponenty liekom BRINEURA. 4 Skontrolujte, či sa na pokožke hlavy nenachádzajú známky unikania tekutiny alebo poruchy pomôcky na intracerebroventrikulárny prístup alebo prejavy možných infekcií (opuch, erytém pokožky hlavy, extravazácia tekutiny alebo vydutie pokožky hlavy okolo pomôcky na intracerebroventrikulárny prístup alebo nad ňou). Nepodávajte liek BRINEURA, ak sa objavia prejavy a príznaky akútneho unikania tekutiny zo zariadenia na intracerebroventrikulárny prístup, zlyhania zariadenia alebo infekcie súvisiacej so zariadením. 5 Pripravte pokožku hlavy na intracerebroventrikulárnu infúziu s použitím aseptického postupu podľa štandardov starostlivosti v danom zdravotníckom zariadení. 6 Zaveďte vstupnú ihlu do zariadenia na intracerebroventrikulárny prístup. 7 K vstupnej ihle pripojte samostatnú prázdnu sterilnú injekčnú striekačku (nie väčšiu ako 3 ml). Naberte 0,5 ml až 1 ml CSF na kontrolu priechodnosti zariadenia na intracerebroventrikulárny prístup. Nevracajte CSF do zariadenia na intracerebroventrikulárny prístup. Vzorky CSF sa majú pravidelne posielať na monitorovanie infekcie. 8 Pripojte infúznu súpravu k vstupnej ihle (pozri obrázok 1). Zaistite komponenty podľa štandardov starostlivosti v danom zdravotníckom zariadení. 9 Vložte injekčnú striekačku obsahujúcu liek BRINEURA do lineárneho dávkovača a naprogramujte ho na rýchlosť podávania infúzie 2,5 ml za hodinu. Alarmy dávkovača naprogramujte tak, aby sa spustili pri najcitlivejších medzných hodnotách tlaku, rýchlosti a objemu. Podrobné informácie sú uvedené v návode na použitie od výrobcu lineárneho dávkovača. Nepodávajte ako bolus ani ručne. 10 Infúziu lieku BRINEURA začnite rýchlosťou 2,5 ml za hodinu. 11 Počas infúzie pravidelne kontrolujte, či infúzny systém nevykazuje známky unikania tekutiny alebo zlyhania podávania. 12 Po skončení infúzie sa presvedčte, či je injekčná striekačka označená ako Brineura v lineárnom dávkovači prázdna. Odpojte a vyberte prázdnu injekčnú striekačku z dávkovača a odpojte ju od hadičky. Prázdnu injekčnú striekačku zlikvidujte v súlade s národnými požiadavkami. 6
7 INTRACEREBROVENTRIKULÁRNA INFÚZIA PREPLACHOVACIEHO ROZTOKU Preplachovací roztok podávajte po dokončení infúzie lieku BRINEURA. 1 Pripojte injekčnú striekačku obsahujúcu vypočítaný objem preplachovacieho roztoku k infúznym komponentom 2 Vložte injekčnú striekačku obsahujúcu preplachovací roztok do lineárneho dávkovača a naprogramujte ho na rýchlosť podávania infúzie 2,5 ml za hodinu. Alarmy dávkovača naprogramujte tak, aby sa spustili pri najcitlivejších medzných hodnotách tlaku, rýchlosti a objemu. Podrobné informácie sú uvedené v návode na použitie od výrobcu lineárneho dávkovača. Nepodávajte ako bolus ani ručne. 3 Infúziu lieku preplachovacieho roztoku začnite rýchlosťou 2,5 ml za hodinu. 4 Počas infúzie pravidelne kontrolujte, či infúzne komponenty nevykazujú známky unikania tekutiny alebo zlyhania podávania. 5 Po skončení infúzie sa presvedčte, či je injekčná striekačka označená ako preplachovací roztok v lineárnom dávkovači prázdna. Odpojte a vyberte prázdnu injekčnú striekačku z dávkovača a odpojte ju od infúznej hadičky. 6 Odstráňte vstupnú ihlu. Jemne stlačte a obviažte miesto podania infúzie podľa štandardov starostlivosti v danom zdravotníckom zariadení. 7 Infúzne komponenty, ihly, nepoužité roztoky a iné odpadové materiály zlikvidujte v súlade s národnými požiadavkami. 7
8 Skrátené informácie o predpisovaní: BRINEURA (cerliponáza alfa) Kompletné informácie nájdete v súhrne charakteristických vlastností lieku. Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili akékoľvek podozrenia na nežiaduce reakcie. Názov lieku: BRINEURA (cerliponáza alfa ) 150 mg infúzny roztok. Zloženie: Každá injekčná liekovka lieku BRINEURA obsahuje 150 mg cerliponázy alfa v 5 ml roztoku (30 mg/ml). Každé balenie obsahuje 2 injekčné liekovky s cerliponázou alfa a jednu injekčnú liekovku preplachovacieho roztoku. Cerliponáza alfa je rekombinantná forma ľudskej tripeptidylpeptidázy 1 (rhtpp1). Terapeutické indikácie: BRINEURA je indikovaná na liečbu ochorenia neuronálna ceroidná lipofuscinóza typu 2 (CLN2), známeho aj ako deficit tripeptidylpeptidázy 1 (TPP1). Dávkovanie a spôsob podávania: BRINEURA smie podávať len vyškolený zdravotnícky pracovník s poznatkami o intracerebroventrikulárnom podávaní v zdravotníckom zariadení. Odporúčaná dávka je 300 mg cerliponázy alfa, ktorá sa podáva jedenkrát za dva týždne intracerebroventrikulárnou infúziou. U pacientov mladších ako 2 roky sa odporúčajú nižšie dávky, pozri úplné znenie súhrnu charakteristických vlastností lieku. BRINEURA a preplachovací roztok sa smú podávať len intracerebroventrikulárnou cestou. Každá injekčná liekovka lieku BRINEURA a preplachovacieho roztoku je určená len na jednorazové použitie. BRINEURA sa podáva do mozgovomiechového moku (cerebrospinal fluid -CSF) infúziou cez chirurgicky implantovaný zásobník a katéter (zariadenie na intracerebroventrikulárny prístup). Zariadenie na intracerebroventrikulárny prístup sa musí implantovať pred prvou infúziou. Implantované zariadenie na intracerebroventrikulárny prístup má byť vhodné na vytvorenie prístupu do mozgových komôr na účely terapeutického podávania. Kontraindikácie: Život ohrozujúca anafylaktická reakcia na liečivo alebo na ktorúkoľvek z pomocných látok, keď pokusy o opätovné nasadenie boli neúspešné. Pacienti s CLN2 s ventrikuloperitoneálnymi skratmi. BRINEURA sa nesmie podávať v prípade známok akútneho unikania tekutiny zo zariadenia na intracerebroventrikulárny prístup, poruchy zariadenia alebo infekcie súvisiacej so zariadením. Osobitné upozornenia a opatrenia pri používaní: BRINEURA sa musí podávať aseptickým postupom, aby sa znížilo riziko infekcie. V klinických štúdiách sa pozorovali prípady infekcií súvisiacich so zariadením na intracerebroventrikulárny prístup. V týchto prípadoch sa podali antibiotiká, zariadenie na intracerebroventrikulárny prístup sa vymenilo a pokračovalo sa v liečbe liekom BRINEURA. Zdravotnícki pracovníci majú pred každou infúziou skontrolovať celistvosť kože pokožky hlavy, aby sa uistili, že zariadenie na intracerebroventrikulárny prístup je neporušené. Pred začatím infúzie lieku BRINEURA sa musí vykonať kontrola miesta podania infúzie a kontrola priechodnosti, aby sa zistilo prípadné unikanie tekutiny zo zariadenia na intracerebroventrikulárny prístup a/alebo jeho porucha. Na potvrdenie neporušenosti zariadenia môže byť potrebná konzultácia s neurochirurgom. Liečba liekom BRINEURA sa má v prípade poruchy zariadenia prerušiť a pred ďalšími infúziami bude možno potrebné zariadenie na prístup vymeniť. V prípade komplikácií súvisiacich so zariadením na intracerebroventrikulárny prístup nájdete ďalšie pokyny na označení obalu zariadenia od výrobcu. Opatrnosť je potrebná u pacientov náchylných na komplikácie v dôsledku podávania intracerebroventrikulárneho lieku vrátane pacientov s obštrukčným hydrocefalom. Nežiaduce účinky: Veľmi časté nežiaduce reakcie zahŕňajú infekciu horných dýchacích ciest, precitlivenosť, podráždenosť, príhody kŕčov, bolesť hlavy, pleocytózu CSF, vracanie, pyrexiu, zvýšenú hladinu proteínu v CSF, abnormality v EKG, pokles proteínu v CSF a problém s ihlou. Časté nežiaduce reakcie zahŕňajú konjuktivitídu, infekciu súvisiacu so zariadením, bradykardiu, syndróm poklesnutej hlavy, bolesť brucha, pľuzgiere na ústnej sliznici, pľuzgiere na jazyku, porucha gastrointestinálneho traktu, vyrážka, urtikária, pocit napätia, bolesť, unikanie tekutiny zo zariadenia a upchatie zariadenia. Dislokácia zariadenia bola hlásenia s neznámou frekvenciou výskytu. Kŕče sú častým prejavom ochorenia CLN2 a ich výskyt v tejto populácii sa očakáva. Celkovo sa udalosť, ktorá zodpovedala štandardizovanému záznamu kŕče v databáze MedDRA, vyskytla u 23 (96 %) účastníkov, ktorí dostali cerliponázu alfa. Medzi najčastejšie hlásené udalosti kŕčov patrí záchvat, epilepsia a celkový tonicko-klonický záchvat. Celkový výskyt udalostí kŕčov s časovým vzťahom k podaniu cerliponázy alfa bol 17 %, pričom udalosti boli mierne až stredne závažné so stupňom závažnosti 1 alebo 2. Spolu 6 % všetkých udalostí kŕčov sa považovalo za súvisiace s cerliponázou alfa, pričom boli mierne až závažné so stupňom CTCAE 1-4. Kŕče ustúpili po podaní štandardných antikonvulzív a neviedli k prerušeniu liečby liekom BRINEURA. Reakcie z precitlivenosti boli hlásené u 14 z 24 pacientov (58 %) liečených liekom BRINEURA. Závažné (stupeň 3 podľa spoločných terminologických kritérií pre nežiaduce udalosti (CTCAE)) reakcie z precitlivenosti sa vyskytli u troch pacientov, pričom u žiadneho pacienta sa liečba neprerušila. Najčastejšie prejavy zahŕňali pyrexiu s vracaním, pleocytózu alebo podráždenosť, čo nezodpovedá klasickej precitlivenosti vyvolanej imunitným systémom. Tieto nežiaduce reakcie sa pozorovali počas infúzie lieku BRINEURA alebo do 24 hodín od jej skončenia a nenarušili liečbu. Príznaky ustúpili časom alebo po podaní antipyretík, antihistaminík a/ alebo glukokortikosteroidov. Zoznam pomocných látok: heptahydrát hydrogenfosforečnanu sodného, monohydrát dihydrogenfosforečnanu sodného, chlorid sodný, chlorid draselný, hexahydrát chloridu horečnatého, dihydrát chloridu vápenatého, voda na injekciu. Inkompatibility: Tento liek sa nesmie miešať s inými liekmi. Uchovávanie a používanie: Uchovávajte vo zvislej polohe v mrazničke (-25 C to -15 C). Rozmrazená BRINEURA a preplachovací roztok sa majú ihneď použiť. Liek sa má odobrať z neotvorených injekčných liekoviek až bezprostredne pred použitím. Ak okamžité použitie nie je možné, neotvorené injekčné liekovky lieku BRINEURA alebo preplachovacieho roztoku sa majú uchovávať pri teplote 2-8 C a použiť do 24 hodín. Príprava infúzie lieku BRINEURA : Pozri úplné znenie súhrnu charakteristických vlastností lieku. Právna klasifikácia: Liek je viazaný na lekársky predpis. Držiteľ rozhodnutia o registrácii: BioMarin International Limited, Shanbally, Ringaskiddy, County Cork, Írsko. Registračné číslo (čísla): EU/1/17/1192/001 Dátum prvej registrácie: 30. mája 2017 Dátum revízie textu: jún BRINEURA je ochranná známka spoločnosti BioMarin Pharmaceutical Inc., u ktorej sú dostupné ďalšie informácie. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili nežiaduce udalosti v súlade s miestnymi predpismi. Nežiaduce udalosti je potrebné hlásiť aj spoločnosti BioMarin na tel. č alebo om na drugsafety@bmrn.com Referencie: 1. Súhrn charakteristických vlastností lieku BRINEURA BioMarin International Ltd. Všetky práva vyhradené. EU/BRIN/0172 December 2017
Dexamed Art 29_Annex I_sk
 Príloha III Zmeny Súhrnu charakteristických vlastností lieku a písomnej informácie pre používateľa Poznámka: Tieto zmeny sa majú zahrnúť do platného Súhrnu charakteristických vlastností lieku, označenia
Príloha III Zmeny Súhrnu charakteristických vlastností lieku a písomnej informácie pre používateľa Poznámka: Tieto zmeny sa majú zahrnúť do platného Súhrnu charakteristických vlastností lieku, označenia
Cymevene IV, INN: ganciclovir
 Príloha II Vedecké závery a odôvodnenie zmeny v podmienkach povolenia na uvedenie lieku na trh 7 Vedecké závery Celkový súhrn vedeckého hodnotenia lieku Cymevene i.v. a súvisiace názvy (pozri prílohu I)
Príloha II Vedecké závery a odôvodnenie zmeny v podmienkach povolenia na uvedenie lieku na trh 7 Vedecké závery Celkový súhrn vedeckého hodnotenia lieku Cymevene i.v. a súvisiace názvy (pozri prílohu I)
Dôležité informácie - Nevyhadzujte! Agomelatine G.L. Pharma 25 mg na liečbu epizód veľkej depresie u dospelých Príručka pre pacienta Verzia 1.0 Schvál
 Dôležité informácie - Nevyhadzujte! Agomelatine G.L. Pharma 25 mg na liečbu epizód veľkej depresie u dospelých Príručka pre pacienta 1 Informácie o tomto lieku Agomelatín je antidepresívum, ktoré je účinné
Dôležité informácie - Nevyhadzujte! Agomelatine G.L. Pharma 25 mg na liečbu epizód veľkej depresie u dospelých Príručka pre pacienta 1 Informácie o tomto lieku Agomelatín je antidepresívum, ktoré je účinné
SW
 Písomná informácia pre používateľa VELETRI 0,5 mg prášok na infúzny roztok VELETRI 1,5 mg prášok na infúzny roztok epoprostenol Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete používať
Písomná informácia pre používateľa VELETRI 0,5 mg prášok na infúzny roztok VELETRI 1,5 mg prášok na infúzny roztok epoprostenol Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete používať
Návod na použitie S Súprava striekačiek Vertecem V+ Nástroje a implantáty schválené nadáciou AO
 Návod na použitie 03.702.215S Súprava striekačiek Vertecem V+ Nástroje a implantáty schválené nadáciou AO Návod na použitie Pred použitím si prečítajte tento návod na použitie, všetky priložené informácie
Návod na použitie 03.702.215S Súprava striekačiek Vertecem V+ Nástroje a implantáty schválené nadáciou AO Návod na použitie Pred použitím si prečítajte tento návod na použitie, všetky priložené informácie
PRAKTICKÉ INFORMÁCIE PRE PACIENTOV LUMBÁLNA PUNKCIA
 PRAKTICKÉ INFORMÁCIE PRE PACIENTOV LUMBÁLNA PUNKCIA ČO JE LUMBÁLNA PUNKCIA? Lumbálna punkcia je vyšetrovacia metóda, pri ktorej sa z diagnostických alebo liečebných dôvodov zavádza do chrbticového kanála
PRAKTICKÉ INFORMÁCIE PRE PACIENTOV LUMBÁLNA PUNKCIA ČO JE LUMBÁLNA PUNKCIA? Lumbálna punkcia je vyšetrovacia metóda, pri ktorej sa z diagnostických alebo liečebných dôvodov zavádza do chrbticového kanála
Familiárna Stredomorská Horúčka Verzia DIAGNÓZA A LIEČBA 2.1 Ako sa choroba diagnostikuj
 https://www.printo.it/pediatric-rheumatology/sk/intro Familiárna Stredomorská Horúčka Verzia 2016 2. DIAGNÓZA A LIEČBA 2.1 Ako sa choroba diagnostikuje? Vo všeobecnosti je postup nasledovný: Klinické podozrenie:
https://www.printo.it/pediatric-rheumatology/sk/intro Familiárna Stredomorská Horúčka Verzia 2016 2. DIAGNÓZA A LIEČBA 2.1 Ako sa choroba diagnostikuje? Vo všeobecnosti je postup nasledovný: Klinické podozrenie:
jfb
 Príloha č. 3 k rozhodnutiu o registrácii lieku, ev.č.: 2009/07643 PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽOV Septolete plus spray orálna aerodisperzia benzokaín/cetylpyridíniumchlorid Pozorne si prečítajte celú
Príloha č. 3 k rozhodnutiu o registrácii lieku, ev.č.: 2009/07643 PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽOV Septolete plus spray orálna aerodisperzia benzokaín/cetylpyridíniumchlorid Pozorne si prečítajte celú
„Chrípka, či prechladnutie“
 Chrípka, či prechladnutie SSVPL SLS, Tatry 2012 * *Medzi prvé príznaky chrípky nepatrí: a) výrazná malátnosť b) silná bolesť hlavy c) serózny sekrét z nosa d) TT do 38 C * *Ktorý typ chrípky nespôsobuje
Chrípka, či prechladnutie SSVPL SLS, Tatry 2012 * *Medzi prvé príznaky chrípky nepatrí: a) výrazná malátnosť b) silná bolesť hlavy c) serózny sekrét z nosa d) TT do 38 C * *Ktorý typ chrípky nespôsobuje
Snímka 1
 Uvedenie zdravotníckej pomôcky na slovenský trh RNDr. Jozef Slaný, MZ SR Seminár Zdravotnícke pomôcky 6. decembra 2017 Austria Trend Hotel Bratislava Zdravotnícke pomôcky Zákon 264/1999 Z. z. o technických
Uvedenie zdravotníckej pomôcky na slovenský trh RNDr. Jozef Slaný, MZ SR Seminár Zdravotnícke pomôcky 6. decembra 2017 Austria Trend Hotel Bratislava Zdravotnícke pomôcky Zákon 264/1999 Z. z. o technických
Schválený text k rozhodnutiu o registrácii, ev
 Schválený text k rozhodnutiu o registrácii, ev. č.: 2015/04965-REG Písomná informácia pre používateľa STADATUSSIN kvapky 19 mg/ml perorálne roztokové kvapky pentoxyverín Pozorne si prečítajte celú písomnú
Schválený text k rozhodnutiu o registrácii, ev. č.: 2015/04965-REG Písomná informácia pre používateľa STADATUSSIN kvapky 19 mg/ml perorálne roztokové kvapky pentoxyverín Pozorne si prečítajte celú písomnú
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV VETERINÁRNEHO LIEKU Porcilis ColiClos injekčná suspenzia pre prasatá 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna dávka 2 ml obsahuje: Účinné
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV VETERINÁRNEHO LIEKU Porcilis ColiClos injekčná suspenzia pre prasatá 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna dávka 2 ml obsahuje: Účinné
nnn
 Schválený text k rozhodnutiu o zmene v registrácii lieku, ev. č.: 2011/04206 Písomná informácia pre používateľa Flumazenil Pharmaselect 0,1 mg/ml injekčný roztok / infúzny koncentrát flumazenil Pozorne
Schválený text k rozhodnutiu o zmene v registrácii lieku, ev. č.: 2011/04206 Písomná informácia pre používateľa Flumazenil Pharmaselect 0,1 mg/ml injekčný roztok / infúzny koncentrát flumazenil Pozorne
Xgeva, INN-denosumab
 B. PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA 28 Písomná informácia pre používateľa XGEVA 120 mg injekčný roztok denosumab Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií
B. PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA 28 Písomná informácia pre používateľa XGEVA 120 mg injekčný roztok denosumab Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií
HYGIENA RÚK
 HYGIENA RÚK Clean care is safer care save lives: clean your hands Súčasťou programu WHO First Global Patient Safety Challenge - Clean Care Is Safer Care je kampaň pod názvom Save Lives: Clean Your Hands
HYGIENA RÚK Clean care is safer care save lives: clean your hands Súčasťou programu WHO First Global Patient Safety Challenge - Clean Care Is Safer Care je kampaň pod názvom Save Lives: Clean Your Hands
Kogenate Bayer, INN- Octocog Alfa
 Príloha IV Vedecké závery a odôvodnenie zmeny v povoleniach na uvedenie na trh 262 Vedecké závery Výbor CHMP vzal na vedomie ďalej uvedené odporúčanie výboru PRAC z 5. decembra 2013 týkajúce sa postupu
Príloha IV Vedecké závery a odôvodnenie zmeny v povoleniach na uvedenie na trh 262 Vedecké závery Výbor CHMP vzal na vedomie ďalej uvedené odporúčanie výboru PRAC z 5. decembra 2013 týkajúce sa postupu
RoActemra, INN-tocilizumab
 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU RoActemra 20 mg/ml infúzny koncentrát. 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každý ml koncentrátu obsahuje 20 mg tocilizumabu* Každá injekčná
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU RoActemra 20 mg/ml infúzny koncentrát. 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každý ml koncentrátu obsahuje 20 mg tocilizumabu* Každá injekčná
Hreferralspcsk
 Schválený text k rozhodnutiu o zmene, ev. číslo: 2015/04702-ZME Písomná informácia pre používateľa Encepur children 0,25 ml injekčnej suspenzie naplnenej v injekčnej striekačke Očkovacia látka proti kliešťovej
Schválený text k rozhodnutiu o zmene, ev. číslo: 2015/04702-ZME Písomná informácia pre používateľa Encepur children 0,25 ml injekčnej suspenzie naplnenej v injekčnej striekačke Očkovacia látka proti kliešťovej
Hreferralspccleansk
 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili
flebaven-500-mg-filmom-obalene-tablety
 Schválený text k rozhodnutiu o registrácii, ev. č.: 2015/07345-REG 1. NÁZOV LIEKU SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU Flebaven 500 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Schválený text k rozhodnutiu o registrácii, ev. č.: 2015/07345-REG 1. NÁZOV LIEKU SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU Flebaven 500 mg filmom obalené tablety 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
H-636-PI-sk
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Myozyme 50 mg prášok na koncentrát na infúzny roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna liekovka obsahuje 50 mg alglukozidázy
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Myozyme 50 mg prášok na koncentrát na infúzny roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna liekovka obsahuje 50 mg alglukozidázy
Blincyto II-09-PI en-tracked
 B. PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA 44 Písomná informácia pre používateľa BLINCYTO 38,5 mikrogramov prášok na prípravu infúzneho koncentrátu a roztok na prípravu infúzneho roztoku blinatumomab Tento
B. PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA 44 Písomná informácia pre používateľa BLINCYTO 38,5 mikrogramov prášok na prípravu infúzneho koncentrátu a roztok na prípravu infúzneho roztoku blinatumomab Tento
Fabrazyme, INN-agalsidase beta
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Fabrazyme 35 mg, prášok na infúzny koncentrát Fabrazyme 5 mg, prášok na infúzny koncentrát 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Fabrazyme 35 mg, prášok na infúzny koncentrát Fabrazyme 5 mg, prášok na infúzny koncentrát 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Ibalgin Duo Effect
 Príloha č. 2 k notifikácii o zmene, ev. č.: 2015/03057-ZIB Písomná informácia pre používateľa Ibalgin DUO EFFECT 5 %/100 UI/mg dermálny krém ibuprofen/heparinoid Pozorne si prečítajte celú písomnú informáciu
Príloha č. 2 k notifikácii o zmene, ev. č.: 2015/03057-ZIB Písomná informácia pre používateľa Ibalgin DUO EFFECT 5 %/100 UI/mg dermálny krém ibuprofen/heparinoid Pozorne si prečítajte celú písomnú informáciu
ZabezpeĊenie protiepidemických opatrení v súvislosti s pandémiou chrípky
 Zabezpečenie protiepidemických opatrení v súvislosti s pandémiou chrípky 14.10.2010 Bratislava J. Pertinačová, epidemiológ RÚVZ Bratislava Cirkulácia vírusu chrípky v populácii epidemický výskyt každý
Zabezpečenie protiepidemických opatrení v súvislosti s pandémiou chrípky 14.10.2010 Bratislava J. Pertinačová, epidemiológ RÚVZ Bratislava Cirkulácia vírusu chrípky v populácii epidemický výskyt každý
Clavudale 50 mg tablet for cats and dogs Article 33(4) referral - Annexes I, II and III
 Príloha I Zoznam názvov, lieková forma, sila veterinárneho lieku, druhy zvierat, cesta podania, žiadateľ/držiteľ povolenia na uvedenie na trh v členských štátoch 1/10 Členský štát EÚ/EHP Žiadateľ/Držiteľ
Príloha I Zoznam názvov, lieková forma, sila veterinárneho lieku, druhy zvierat, cesta podania, žiadateľ/držiteľ povolenia na uvedenie na trh v členských štátoch 1/10 Členský štát EÚ/EHP Žiadateľ/Držiteľ
Písomná informácia pre používateľa RoActemra 20 mg/ml infúzny koncentrát tocilizumab Pozorne si prečítajte celú písomnú informáciu predtým, ako začnet
 Písomná informácia pre používateľa RoActemra 20 mg/ml infúzny koncentrát tocilizumab Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete používať tento liek, pretože obsahuje pre vás dôležité
Písomná informácia pre používateľa RoActemra 20 mg/ml infúzny koncentrát tocilizumab Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete používať tento liek, pretože obsahuje pre vás dôležité
Deficit Mevalonát Kinázy (MKD) (alebo hyper IgD syndróm) Verzia ČO JE MKD? 1.1 Čo to je?
 https://www.printo.it/pediatric-rheumatology/sk/intro Deficit Mevalonát Kinázy (MKD) (alebo hyper IgD syndróm) Verzia 2016 1. ČO JE MKD? 1.1 Čo to je? Deficit mevalonát kinázy je dedičné ochorenie. Je
https://www.printo.it/pediatric-rheumatology/sk/intro Deficit Mevalonát Kinázy (MKD) (alebo hyper IgD syndróm) Verzia 2016 1. ČO JE MKD? 1.1 Čo to je? Deficit mevalonát kinázy je dedičné ochorenie. Je
jfb
 Príloha č. 2 k notifikácii o zmene, ev.č. 2013/04610 Písomná informácia pre používateľa Unipres 10 Unipres 20 nitrendipín Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete užívať tento
Príloha č. 2 k notifikácii o zmene, ev.č. 2013/04610 Písomná informácia pre používateľa Unipres 10 Unipres 20 nitrendipín Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete užívať tento
MINISTERSTVO ZDRAVOTNÍCTVA SLOVENSKEJ REPUBLIKY C (MZ SR) 5-01 ROČNÝ VÝKAZ O ČINNOSTI ALGEZIOLÓGIE za rok 2019 Registrované ŠÚ SR Č. Vk. 960/19 z 5.9.
 MINISTERSTVO ZDRAVOTNÍCTVA SLOVENSKEJ REPUBLIKY C (MZ SR) 5 - ROČNÝ VÝKAZ O ČINNOSTI ALGEZIOLÓGIE za rok 29 Registrované ŠÚ SR Č. Vk. 960/19 z 5.9.28 Ochranu dôverných údajov upravuje zákon č. 540/20 Z.
MINISTERSTVO ZDRAVOTNÍCTVA SLOVENSKEJ REPUBLIKY C (MZ SR) 5 - ROČNÝ VÝKAZ O ČINNOSTI ALGEZIOLÓGIE za rok 29 Registrované ŠÚ SR Č. Vk. 960/19 z 5.9.28 Ochranu dôverných údajov upravuje zákon č. 540/20 Z.
Zodpovedný prístup k rizikám hormonálnej substitučnej liečby a antikoncepcie
 Zodpovedný prístup k rizikám hormonálnej substitučnej liečby a antikoncepcie TROMBOtest je balík laboratórnych vyšetrení, ktorý vám dá jasnú odpoveď, či je vo vašom súčasnom zdravotnom stave vhodné užívať
Zodpovedný prístup k rizikám hormonálnej substitučnej liečby a antikoncepcie TROMBOtest je balík laboratórnych vyšetrení, ktorý vám dá jasnú odpoveď, či je vo vašom súčasnom zdravotnom stave vhodné užívať
Schválený text k rozhodnutiu o predĺžení, ev. č.: 2015/04382-PRE Písomná informácia pre používateľa Paracut 250 mg tablety paracetamol Pozorne si preč
 Písomná informácia pre používateľa Paracut 250 mg tablety paracetamol Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete užívať tento liek, pretože obsahuje pre vás dôležité informácie.
Písomná informácia pre používateľa Paracut 250 mg tablety paracetamol Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete užívať tento liek, pretože obsahuje pre vás dôležité informácie.
Untitled
 R O Z H O D N U T I E Ministerstvo zdravotníctva Slovenskej republiky (ďalej len ministerstvo ) ako príslušný orgán podľa 57 a 65 ods. 1 zákona č. 363/2011 Z. z. o rozsahu a podmienkach úhrady liekov,
R O Z H O D N U T I E Ministerstvo zdravotníctva Slovenskej republiky (ďalej len ministerstvo ) ako príslušný orgán podľa 57 a 65 ods. 1 zákona č. 363/2011 Z. z. o rozsahu a podmienkach úhrady liekov,
„Chrípka, či prechladnutie“
 Chrípka, či prechladnutie SSVPL SLS, jesenný cyklus 2012 Etiologický agens infekcie dýchacích ciest: 1.Vírusy a) ľudské respiračné vírusy - chrípka, rhinovírusy, koronarovírusy, vírus parainfluenzy, respiračný
Chrípka, či prechladnutie SSVPL SLS, jesenný cyklus 2012 Etiologický agens infekcie dýchacích ciest: 1.Vírusy a) ľudské respiračné vírusy - chrípka, rhinovírusy, koronarovírusy, vírus parainfluenzy, respiračný
Optaflu, INN-Influenza vaccine (surface antigen, inactivated, prepared in cell cultures)
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Optaflu injekčná suspenzia v naplnenej injekčnej striekačke Chrípková vakcína (inaktivovaný povrchový antigén pripravený v bunkových
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Optaflu injekčná suspenzia v naplnenej injekčnej striekačke Chrípková vakcína (inaktivovaný povrchový antigén pripravený v bunkových
Repatha, INN-evolocumab
 B. PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA 43 Písomná informácia pre používateľa Repatha 140 mg injekčný roztok naplnený v injekčnej striekačke evolokumab Tento liek je predmetom ďalšieho monitorovania. To
B. PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA 43 Písomná informácia pre používateľa Repatha 140 mg injekčný roztok naplnený v injekčnej striekačke evolokumab Tento liek je predmetom ďalšieho monitorovania. To
Najrozsiahlejší dostupný plán ochrany 1 IBA PRE PRSNÍKOVÉ IMPLANTÁTY MENTOR Ochrana, akú vám nikto iný neposkytne
 Najrozsiahlejší dostupný plán ochrany 1 IBA PRE PRSNÍKOVÉ IMPLANTÁTY MENTOR Ochrana, akú vám nikto iný neposkytne Vaše dlhodobé zdravie je našim záväzkom Sme tu pre vás, aby sme vám pred operáciou odpovedali
Najrozsiahlejší dostupný plán ochrany 1 IBA PRE PRSNÍKOVÉ IMPLANTÁTY MENTOR Ochrana, akú vám nikto iný neposkytne Vaše dlhodobé zdravie je našim záväzkom Sme tu pre vás, aby sme vám pred operáciou odpovedali
Vaxxitek HVT+IBD
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV VETERINÁRNEHO LIEKU Vaxxitek HVT+IBD suspenzia a riedidlo na injekčnú suspenziu 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá dávka vakcíny
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV VETERINÁRNEHO LIEKU Vaxxitek HVT+IBD suspenzia a riedidlo na injekčnú suspenziu 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá dávka vakcíny
Omidria, INN-phenylephrine hydrochloride / ketorolac trometamol
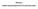 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Omidria 10 mg/ml + 3 mg/ml koncentrát na prípravu roztoku na vnútroočný výplach 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každé 4 ml roztoku
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Omidria 10 mg/ml + 3 mg/ml koncentrát na prípravu roztoku na vnútroočný výplach 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každé 4 ml roztoku
Príloha 2 k Rozhodnutiu o zmene registrácie lieku, ev
 Príloha č. 2 k notifikácii o zmene, ev.č. 2014/03062-ZIB Písomná informácia pre používateľa BRIMONAL 0,2 % očná roztoková instilácia brimonidíniumtartarát Pozorne si prečítajte celú písomnú informáciu
Príloha č. 2 k notifikácii o zmene, ev.č. 2014/03062-ZIB Písomná informácia pre používateľa BRIMONAL 0,2 % očná roztoková instilácia brimonidíniumtartarát Pozorne si prečítajte celú písomnú informáciu
Na základe plánu práce na rok 2018 uskutočnila Slovenská obchodná inšpekcia (ďalej len SOI ) celoslovenskú kontrolnú akciu na hračky, ktorá prebiehala
 Na základe plánu práce na rok 2018 uskutočnila Slovenská obchodná inšpekcia (ďalej len SOI ) celoslovenskú kontrolnú akciu na hračky, ktorá prebiehala do konca novembra 2018. Kontrolná akcia bola zameraná
Na základe plánu práce na rok 2018 uskutočnila Slovenská obchodná inšpekcia (ďalej len SOI ) celoslovenskú kontrolnú akciu na hračky, ktorá prebiehala do konca novembra 2018. Kontrolná akcia bola zameraná
48-CHO-Dz-kraj-teória a prax-riešenie
 SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY CHEMICKÁ OLYMPIÁDA 48. ročník, školský rok 2011/2012 Kategória Dz Krajské kolo RIEŠENIE A HODNOTENIE TEORETICKÝCH A PRAKTICKÝCH ÚLOH RIEŠENIE A HODNOTENIE TEORETICKÝCH
SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY CHEMICKÁ OLYMPIÁDA 48. ročník, školský rok 2011/2012 Kategória Dz Krajské kolo RIEŠENIE A HODNOTENIE TEORETICKÝCH A PRAKTICKÝCH ÚLOH RIEŠENIE A HODNOTENIE TEORETICKÝCH
Flebogamma DIF,INN-Human normal immunoglobulin
 1. NÁZOV LIEKU Flebogamma DIF 100 mg/ml infúzny roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Normálny ľudský imunoglobulín (IVIg) Jeden ml obsahuje: Normálny ľudský imunoglobulín...100 mg (čistota najmenej
1. NÁZOV LIEKU Flebogamma DIF 100 mg/ml infúzny roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Normálny ľudský imunoglobulín (IVIg) Jeden ml obsahuje: Normálny ľudský imunoglobulín...100 mg (čistota najmenej
Kyprolis, INN-carfilzomib
 B. PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA 45 Písomná informácia pre používateľa Kyprolis 10 mg prášok na infúzny roztok Kyprolis 30 mg prášok na infúzny roztok Kyprolis 60 mg prášok na infúzny roztok karfilzomib
B. PÍSOMNÁ INFORMÁCIA PRE POUŽÍVATEĽA 45 Písomná informácia pre používateľa Kyprolis 10 mg prášok na infúzny roztok Kyprolis 30 mg prášok na infúzny roztok Kyprolis 60 mg prášok na infúzny roztok karfilzomib
Flebogamma DIF,INN-Human normal immunoglobulin
 1. NÁZOV LIEKU Flebogamma DIF 50 mg/ml infúzny roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Normálny ľudský imunoglobulín (IVIg) Jeden ml obsahuje: Normálny ľudský imunoglobulín...50 mg (čistota najmenej
1. NÁZOV LIEKU Flebogamma DIF 50 mg/ml infúzny roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Normálny ľudský imunoglobulín (IVIg) Jeden ml obsahuje: Normálny ľudský imunoglobulín...50 mg (čistota najmenej
Učebný plán kurzu prvej pomoci podľa Vyhlášky MZ SR 398/2010 Z.z. Názov predmetu Všeobecné zásady poskytovania prvej pomoci pri dopravných nehodách, š
 Učebný plán kurzu prvej pomoci podľa Vyhlášky MZ SR 398/200 Z.z. Názov predmetu Všeobecné zásady poskytovania prvej pomoci pri dopravných nehodách, športe, náhlych ochoreniach Stavy bezprostredne ohrozujúce
Učebný plán kurzu prvej pomoci podľa Vyhlášky MZ SR 398/200 Z.z. Názov predmetu Všeobecné zásady poskytovania prvej pomoci pri dopravných nehodách, športe, náhlych ochoreniach Stavy bezprostredne ohrozujúce
Nucala, INN-mepolizumab
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje,
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje,
Príloha č
 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU HAVRIX 1440 Dosis adulta HAVRIX 720 Junior monodose Injekčná suspenzia Očkovacia látka proti hepatitíde A (inaktivovaná, adsorbovaná) 2. KVALITATÍVNE
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU HAVRIX 1440 Dosis adulta HAVRIX 720 Junior monodose Injekčná suspenzia Očkovacia látka proti hepatitíde A (inaktivovaná, adsorbovaná) 2. KVALITATÍVNE
Návrh
 Žiadosť o podmienené zaradenie lieku do zoznamu kategorizovaných liekov a úradné určenie ceny lieku Typ žiadosti A1P Časť A Údaje o žiadateľovi 1. Držiteľ registrácie: Meno a priezvisko alebo obchodné
Žiadosť o podmienené zaradenie lieku do zoznamu kategorizovaných liekov a úradné určenie ceny lieku Typ žiadosti A1P Časť A Údaje o žiadateľovi 1. Držiteľ registrácie: Meno a priezvisko alebo obchodné
Blincyto, INN-blinatumomab
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje,
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje,
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU
 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU PABAL 100 mikrogramov/ml injekčný roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Karbetocín 100 mikrogramov/ml. Aktivita oxytocínu: približne 50
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU PABAL 100 mikrogramov/ml injekčný roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Karbetocín 100 mikrogramov/ml. Aktivita oxytocínu: približne 50
NeoRecormon, INN-epoetin beta
 1. NÁZOV LIEKU SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU NeoRecormon na viac dávok 50 000 IU lyofilizát a rozpúšťadlo na injekčný roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna injekčná liekovka
1. NÁZOV LIEKU SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU NeoRecormon na viac dávok 50 000 IU lyofilizát a rozpúšťadlo na injekčný roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna injekčná liekovka
Dostatok energie u chronického ochorenia obličiek a optimálnu telesná hmotnosť - Dieta při chronickém onemocnění ledvin
 Dostatok energie u chronického ochorenia obličiek a optimálnu telesná hmotnosť 5. 3. 2019 Dostatok energie pri chronickom ochorení obličiek a optimálna telesná hmotnosť Zaistenie dostatočného množstva
Dostatok energie u chronického ochorenia obličiek a optimálnu telesná hmotnosť 5. 3. 2019 Dostatok energie pri chronickom ochorení obličiek a optimálna telesná hmotnosť Zaistenie dostatočného množstva
Regulované napájacie zdroje DC AX-3005DBL jednokanálový AX-3005DBL 3-trojkanálový
 Regulované napájacie zdroje DC AX-3005DBL jednokanálový AX-3005DBL 3-trojkanálový Návod na obsluhu Kapitola 1. Inštalácia a odporúčania týkajúce sa používania Počas inštalácie napájacieho zdroja bezpodmienečne
Regulované napájacie zdroje DC AX-3005DBL jednokanálový AX-3005DBL 3-trojkanálový Návod na obsluhu Kapitola 1. Inštalácia a odporúčania týkajúce sa používania Počas inštalácie napájacieho zdroja bezpodmienečne
Príloha č
 SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Pulmozyme 2 500 U/2,5 ml roztok na rozprašovanie 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá ampulka obsahuje 2 500 U (zodpovedá 2,5 mg) dornázy
SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1. NÁZOV LIEKU Pulmozyme 2 500 U/2,5 ml roztok na rozprašovanie 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každá ampulka obsahuje 2 500 U (zodpovedá 2,5 mg) dornázy
KVETNÁ BRATISLAVA 26 Porovnanie zákonov o liekoch a zdravotníckych pomôckach a o zmene a doplnení niektorých zákonov klinické skúšanie humán
 KVETNÁ 11 825 08 BRATISLAVA 26 Porovnanie zákonov o liekoch a zdravotníckych pomôckach a o zmene a doplnení niektorých zákonov klinické skúšanie humánnych liekov Zákon 140/1998 Z.z. účinný do 30.11.2011
KVETNÁ 11 825 08 BRATISLAVA 26 Porovnanie zákonov o liekoch a zdravotníckych pomôckach a o zmene a doplnení niektorých zákonov klinické skúšanie humánnych liekov Zákon 140/1998 Z.z. účinný do 30.11.2011
RIEŠENIE A HODNOTENIE ÚLOH Z PRAKTICKEJ ČASTI
 SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY CHEMICKÁ OLYMPIÁDA 5. ročník, školský rok 015/016 Kategória C Domáce kolo RIEŠENIE A HODNOTENIE PRAKTICKÝCH ÚLOH RIEŠENIE A HODNOTENIE ÚLOH PRAKTICKEJ ČASTI Chemická
SLOVENSKÁ KOMISIA CHEMICKEJ OLYMPIÁDY CHEMICKÁ OLYMPIÁDA 5. ročník, školský rok 015/016 Kategória C Domáce kolo RIEŠENIE A HODNOTENIE PRAKTICKÝCH ÚLOH RIEŠENIE A HODNOTENIE ÚLOH PRAKTICKEJ ČASTI Chemická
NovoRapid, INN-insulin aspart
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU NovoRapid 100 jednotiek/ml injekčný roztok v injekčnej liekovke NovoRapid Penfill 100 jednotiek/ml injekčný roztok v náplni NovoRapid
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU NovoRapid 100 jednotiek/ml injekčný roztok v injekčnej liekovke NovoRapid Penfill 100 jednotiek/ml injekčný roztok v náplni NovoRapid
Adresa príslušnej zdravotnej poisťovne: Obchodné meno Ulica/č. Mesto PSČ Žiadosť o udelenie súhlasu podľa 9f ods. 1 zákona č. 580/2004 Z. z. o zdravot
 Adresa príslušnej zdravotnej poisťovne: Obchodné meno Ulica/č. Mesto PSČ Žiadosť o udelenie súhlasu podľa 9f ods. 1 zákona č. 580/2004 Z. z. o zdravotnom poistení a o zmene a doplnení zákona č. 95/2002
Adresa príslušnej zdravotnej poisťovne: Obchodné meno Ulica/č. Mesto PSČ Žiadosť o udelenie súhlasu podľa 9f ods. 1 zákona č. 580/2004 Z. z. o zdravotnom poistení a o zmene a doplnení zákona č. 95/2002
Kazuistika 1
 Liečba idiopatickej membránovej GN Adrián Okša LF SZU Bratislava Membránová GN najčastejšia príčina nefrotického syndrómu u dospelých v Európe incidencia 5-10/milión obyv./rok primárna (idiopatická) 60-80
Liečba idiopatickej membránovej GN Adrián Okša LF SZU Bratislava Membránová GN najčastejšia príčina nefrotického syndrómu u dospelých v Európe incidencia 5-10/milión obyv./rok primárna (idiopatická) 60-80
Mixtard, INN-insulin human (rDNA)
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Mixtard 30 40 medzinárodných jednotiek/ml injekčná suspenzia v injekčnej liekovke Mixtard 30 100 medzinárodných jednotiek/ml injekčná
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Mixtard 30 40 medzinárodných jednotiek/ml injekčná suspenzia v injekčnej liekovke Mixtard 30 100 medzinárodných jednotiek/ml injekčná
Príloha č
 1. NÁZOV LIEKU SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU ENGERIX-B 20 μg 20 mikrogramov/1 ml, injekčná suspenzia Očkovacia látka proti hepatitíde B (rdna, adsorbovaná) 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
1. NÁZOV LIEKU SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU ENGERIX-B 20 μg 20 mikrogramov/1 ml, injekčná suspenzia Očkovacia látka proti hepatitíde B (rdna, adsorbovaná) 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
CODFR09024sk03v03.qxd:CODFRO5041sk03v02.qxd
 CODFR09024sk03v03.qxd : CODFRO5041sk03v02.qxd, Flat 1 of 18 - Pages: 36, 1, 04/10/09 12:42 AM Cyan Magenta Yellow Black DÔLEŽITÉ INFORMÁCIE Pred použitím výrobku si prečítajte tieto informácie Implantovateľná
CODFR09024sk03v03.qxd : CODFRO5041sk03v02.qxd, Flat 1 of 18 - Pages: 36, 1, 04/10/09 12:42 AM Cyan Magenta Yellow Black DÔLEŽITÉ INFORMÁCIE Pred použitím výrobku si prečítajte tieto informácie Implantovateľná
S L O V E N S K Ý P A R A L Y M P I J S K Ý V Ý B O R B e n e d i k t i h o 5, B r a t i s l a v a ŠPORTOVO-ZDRAVOTNÁ KLASIFIKÁCIA ŽIAKOV SO ZD
 S L O V E N S K Ý P A R A L Y M P I J S K Ý V Ý B O R B e n e d i k t i h o 5, 811 05 B r a t i s l a v a ŠPORTOVO-ZDRAVOTNÁ KLASIFIKÁCIA ŽIAKOV SO ZDRAVOTNÝM ZNEVÝHODNENÍM V Bratislave 15.1.2018 1. Športovo-zdravotná
S L O V E N S K Ý P A R A L Y M P I J S K Ý V Ý B O R B e n e d i k t i h o 5, 811 05 B r a t i s l a v a ŠPORTOVO-ZDRAVOTNÁ KLASIFIKÁCIA ŽIAKOV SO ZDRAVOTNÝM ZNEVÝHODNENÍM V Bratislave 15.1.2018 1. Športovo-zdravotná
2012 PARI GmbH Spezialisten für effektive Inhalation, 035D2003-A-08/12 2
 2012 PARI GmbH Spezialisten für effektive Inhalation, 035D2003-A-08/12 2 3 sk Návod na použitie na domáce použitie 1 DÔLEŽITÉ UPOZORNENIA Dôkladne si prečítajte tento návod na použitie. Uschovajte si ho
2012 PARI GmbH Spezialisten für effektive Inhalation, 035D2003-A-08/12 2 3 sk Návod na použitie na domáce použitie 1 DÔLEŽITÉ UPOZORNENIA Dôkladne si prečítajte tento návod na použitie. Uschovajte si ho
Schválený text k rozhodnutiu o registrácii lieku, ev.č.: 2012/01300 Písomná informácia pre používateľa Tolnexa 20 mg/ml infúzny koncentrát 20 mg/1 ml
 Schválený text k rozhodnutiu o registrácii lieku, ev.č.: 2012/01300 Písomná informácia pre používateľa Tolnexa 20 mg/ml infúzny koncentrát 20 mg/1 ml infúzny koncentrát 80 mg/4 ml infúzny koncentrát 160
Schválený text k rozhodnutiu o registrácii lieku, ev.č.: 2012/01300 Písomná informácia pre používateľa Tolnexa 20 mg/ml infúzny koncentrát 20 mg/1 ml infúzny koncentrát 80 mg/4 ml infúzny koncentrát 160
Ako vymeniť palivový filter na KIA SORENTO BL
 Ako vymeniť palivový filter na Výmenu uskutočnite v nasledujúcom poradí: 1 Zaistite adekvátnu ventiláciu na pracovisku. Výpary z paliva sú jedovaté. Otvorte kapotu 2.1 2.2 Odstráňte kryt motora 2.3 2.4
Ako vymeniť palivový filter na Výmenu uskutočnite v nasledujúcom poradí: 1 Zaistite adekvátnu ventiláciu na pracovisku. Výpary z paliva sú jedovaté. Otvorte kapotu 2.1 2.2 Odstráňte kryt motora 2.3 2.4
Na základe plánu práce na 2. polrok 2017 uskutočnila Slovenská obchodná inšpekcia (ďalej len SOI ) celoslovenskú kontrolnú akciu na hračky. Bola zamer
 Na základe plánu práce na 2. polrok 2017 uskutočnila Slovenská obchodná inšpekcia (ďalej len SOI ) celoslovenskú kontrolnú akciu na hračky. Bola zameraná na dodržiavanie informačných povinností, označenia
Na základe plánu práce na 2. polrok 2017 uskutočnila Slovenská obchodná inšpekcia (ďalej len SOI ) celoslovenskú kontrolnú akciu na hračky. Bola zameraná na dodržiavanie informačných povinností, označenia
Apidra, INN-insulin glulisin
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Apidra 100 jednotiek/ml injekčný roztok v injekčnej liekovke Apidra 100 jednotiek/ml injekčný roztok v náplni Apidra SoloStar 100 jednotiek/ml
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Apidra 100 jednotiek/ml injekčný roztok v injekčnej liekovke Apidra 100 jednotiek/ml injekčný roztok v náplni Apidra SoloStar 100 jednotiek/ml
tabulky_ko-2017-knm
 ZÁKLADNÉ OČKOVANIE PROTI ZÁŠKRTU, TETANU, ČIERNEMU KAŠLU, VÍRUSOVEJ HEPATITÍDE B, HEMOFILOVÝM INVAZÍVNYM INFEKCIÁM, DETSKEJ OBRNE A PNEUMOKOKOVÝM INVAZÍVNYM OCHORENIAM K 31. 8. 2017 V SR Ročník narodenia
ZÁKLADNÉ OČKOVANIE PROTI ZÁŠKRTU, TETANU, ČIERNEMU KAŠLU, VÍRUSOVEJ HEPATITÍDE B, HEMOFILOVÝM INVAZÍVNYM INFEKCIÁM, DETSKEJ OBRNE A PNEUMOKOKOVÝM INVAZÍVNYM OCHORENIAM K 31. 8. 2017 V SR Ročník narodenia
Príloha č
 PODROBNOSTI O FAKTOROCH PRÁCE A PRACOVNÉHO PROSTREDIA PODĽA ZARADENIA PRÁC DO KATEGÓRIÍ A. Hluk 1 ) a) Práce, pri ktorých je predpoklad, že normalizovaná hladina expozície hluku L AEX,8h neprekročí 75
PODROBNOSTI O FAKTOROCH PRÁCE A PRACOVNÉHO PROSTREDIA PODĽA ZARADENIA PRÁC DO KATEGÓRIÍ A. Hluk 1 ) a) Práce, pri ktorých je predpoklad, že normalizovaná hladina expozície hluku L AEX,8h neprekročí 75
(Microsoft PowerPoint Lie\350ebn\351 vyu\236itie PF.ppt [iba na \350\355tanie])
![(Microsoft PowerPoint Lie\350ebn\351 vyu\236itie PF.ppt [iba na \350\355tanie]) (Microsoft PowerPoint Lie\350ebn\351 vyu\236itie PF.ppt [iba na \350\355tanie])](/thumbs/100/145225881.jpg) Liečebné využitie plazmaferézy z pohľadu sestry Dipl. sestra Edita Kohútová Dipl. sestra Renáta Rovenská XVIII. Celoslovenská konferencia sekcie sestier pracujúcich v nefrológii Patince 23. 25. september
Liečebné využitie plazmaferézy z pohľadu sestry Dipl. sestra Edita Kohútová Dipl. sestra Renáta Rovenská XVIII. Celoslovenská konferencia sekcie sestier pracujúcich v nefrológii Patince 23. 25. september
Aimovig, INN-erenumab
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje,
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje,
PRÍLOHA I
 Písomná informácia pre používateľa Ebixa 10 mg filmom obalené tablety Memantínchlorid Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete užívať tento liek, pretože obsahuje pre vás dôležité
Písomná informácia pre používateľa Ebixa 10 mg filmom obalené tablety Memantínchlorid Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete užívať tento liek, pretože obsahuje pre vás dôležité
UBAC
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV VETERINÁRNEHO LIEKU UBAC injekčná emulzia pre hovädzí dobytok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna dávka (2 ml) obsahuje: Účinná
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV VETERINÁRNEHO LIEKU UBAC injekčná emulzia pre hovädzí dobytok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna dávka (2 ml) obsahuje: Účinná
Vždy pripravení pomôcť Zaregistrujte svoj produkt a získajte podporu na SPA2100 Príručka užívateľa
 Vždy pripravení pomôcť Zaregistrujte svoj produkt a získajte podporu na www.philips.com/welcome SPA2100 Príručka užívateľa Obsah 1 Bezpečnosť 2 Dôležité bezpečnostné pokyny 2 2 Upozornenie 2 Recyklácia
Vždy pripravení pomôcť Zaregistrujte svoj produkt a získajte podporu na www.philips.com/welcome SPA2100 Príručka užívateľa Obsah 1 Bezpečnosť 2 Dôležité bezpečnostné pokyny 2 2 Upozornenie 2 Recyklácia
Externé mediálne karty Používateľská príručka
 Externé mediálne karty Používateľská príručka Copyright 2006 Hewlett-Packard Development Company, L.P. Logo SD je obchodná známka svojho vlastníka. Java je obchodná známka spoločnosti Sun Microsystems,
Externé mediálne karty Používateľská príručka Copyright 2006 Hewlett-Packard Development Company, L.P. Logo SD je obchodná známka svojho vlastníka. Java je obchodná známka spoločnosti Sun Microsystems,
Vždy pripravení pomôcť Zaregistrujte svoj produkt a získajte podporu na lokalite Otázky? Kontaktujte Philips SPA20 Príručka už
 Vždy pripravení pomôcť Zaregistrujte svoj produkt a získajte podporu na lokalite www.philips.com/welcome Otázky? Kontaktujte Philips SPA20 Príručka užívateľa Obsah 1 Dôležité 3 2 Upozornenie 4 3 Váš multimediálny
Vždy pripravení pomôcť Zaregistrujte svoj produkt a získajte podporu na lokalite www.philips.com/welcome Otázky? Kontaktujte Philips SPA20 Príručka užívateľa Obsah 1 Dôležité 3 2 Upozornenie 4 3 Váš multimediálny
Návod na obsluhu Ultrazvukový reflexný spínač bez IO- Link SK UGT20x UGT21x UGT50x UGT52x / / 2019
 Návod na obsluhu Ultrazvukový reflexný spínač bez IO- ink UGTx UGTx UGT5x UGT5x 8775 / / 9 Bezpečnostné upozornenia Tento dokument si pred uvedením prístroja do prevádzky prečítajte a počas používania
Návod na obsluhu Ultrazvukový reflexný spínač bez IO- ink UGTx UGTx UGT5x UGT5x 8775 / / 9 Bezpečnostné upozornenia Tento dokument si pred uvedením prístroja do prevádzky prečítajte a počas používania
Reklamačný poriadok Článok I ÚVODNÉ USTANOVENIA 1. Spoločnosť thiss s.r.o., so sídlom Mlynské Nivy 56, Bratislava, IČO: , zapísaná v
 Reklamačný poriadok Článok I ÚVODNÉ USTANOVENIA 1. Spoločnosť thiss s.r.o., so sídlom Mlynské Nivy 56, 821 05 Bratislava, IČO: 47 669 217, zapísaná v Obchodnom registri Okresného súdu Bratislava I, oddiel
Reklamačný poriadok Článok I ÚVODNÉ USTANOVENIA 1. Spoločnosť thiss s.r.o., so sídlom Mlynské Nivy 56, 821 05 Bratislava, IČO: 47 669 217, zapísaná v Obchodnom registri Okresného súdu Bratislava I, oddiel
Empliciti, INN-elotuzumab
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje,
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 Tento liek je predmetom ďalšieho monitorovania. To umožní rýchle získanie nových informácií o bezpečnosti. Od zdravotníckych pracovníkov sa vyžaduje,
Microsoft Word - PIL doc
 Písomná informácia pre používateľa Cefepím Noridem 1 g prášok na injekčný/infúzny roztok Cefepím Noridem 2 g prášok na injekčný/infúzny roztok cefepím Pozorne si prečítajte celú písomnú informáciu predtým,
Písomná informácia pre používateľa Cefepím Noridem 1 g prášok na injekčný/infúzny roztok Cefepím Noridem 2 g prášok na injekčný/infúzny roztok cefepím Pozorne si prečítajte celú písomnú informáciu predtým,
Luminity, INN-perflutren
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Luminity 150 mikrolitrov/ml plyn a rozpúšťadlo na injekčnú/infúznu disperziu 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každý ml obsahuje
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Luminity 150 mikrolitrov/ml plyn a rozpúšťadlo na injekčnú/infúznu disperziu 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každý ml obsahuje
Microsoft Word - Mycamine PIL_SK_07_2018.docx
 Písomná informácia pre používateľa Mycamine 50 mg prášok na infúzny roztok Mycamine 100 mg prášok na infúzny roztok mikafungín Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete používať
Písomná informácia pre používateľa Mycamine 50 mg prášok na infúzny roztok Mycamine 100 mg prášok na infúzny roztok mikafungín Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete používať
Multifunkční hrnec R-292 halogen
 Návod na použitie ČISTIČKA VZDUCHU DO AUTA R-9100 Pred použitím tohto spotrebiča sa prosím zoznámte s návodom na jeho obsluhu. Spotrebič používajte iba tak, ako je popísané v tomto návode na použitie.
Návod na použitie ČISTIČKA VZDUCHU DO AUTA R-9100 Pred použitím tohto spotrebiča sa prosím zoznámte s návodom na jeho obsluhu. Spotrebič používajte iba tak, ako je popísané v tomto návode na použitie.
Microsoft Word _REG_EU_SK.DOC
 ODDIEL 0. VŠEOBECNÉ INFORMÁCIE Tieto produkty sa považujú za druhy tovaru podla clánku 3.3 nariadenia (ES) c. 1907/2006 (REACH). Neobsahujú látky, ktoré by sa mohli uvolnit za normálnych alebo racionálne
ODDIEL 0. VŠEOBECNÉ INFORMÁCIE Tieto produkty sa považujú za druhy tovaru podla clánku 3.3 nariadenia (ES) c. 1907/2006 (REACH). Neobsahujú látky, ktoré by sa mohli uvolnit za normálnych alebo racionálne
Stelara, INN-ustekinumab
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU STELARA 130 mg koncentrát na infúzny roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna injekčná liekovka obsahuje 130 mg ustekinumabu
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU STELARA 130 mg koncentrát na infúzny roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Jedna injekčná liekovka obsahuje 130 mg ustekinumabu
Ako vymeniť tlmiče prednej nápravy na Opel Astra H
 Výmenu uskutočnite v nasledujúcom poradí: 1 Vymeňte zároveň oba tlmiče v rámci opravy vášho auta Opel Astra H. 2 Pod zadné kolesá umiestnite kliny. 4 Zodvihnite prednú časť vozidla a zaistite vozidlo na
Výmenu uskutočnite v nasledujúcom poradí: 1 Vymeňte zároveň oba tlmiče v rámci opravy vášho auta Opel Astra H. 2 Pod zadné kolesá umiestnite kliny. 4 Zodvihnite prednú časť vozidla a zaistite vozidlo na
ÚRAD VEREJNÉHO ZDRAVOTNÍCTVA SLOVENSKEJ REPUBLIKY Trnavská cesta 52 P.O.BOX Bratislava TASR, SITA Vaša značka/zo dňa Naša značka Vybavuje Br
 ÚRAD VEREJNÉHO ZDRAVOTNÍCTVA SLOVENSKEJ REPUBLIKY Trnavská cesta 52 P.O.BOX 45 826 45 Bratislava TASR, SITA Vaša značka/zo dňa Naša značka Vybavuje Bratislava -/- OHVBPKV/5249-4/18332/2018/Ki Ing. Kišacová,
ÚRAD VEREJNÉHO ZDRAVOTNÍCTVA SLOVENSKEJ REPUBLIKY Trnavská cesta 52 P.O.BOX 45 826 45 Bratislava TASR, SITA Vaša značka/zo dňa Naša značka Vybavuje Bratislava -/- OHVBPKV/5249-4/18332/2018/Ki Ing. Kišacová,
Microsoft Word - Li-Fraumeni syndrom.docx
 VAŠA DNA ANALÝZA Čo je Li- Fraumeni syndróm? Syndróm Li-Fraumeni je vrodené autozomálne dominantné ochorenie. Vzniká najčastejšie na podklade mutácie génu TP53. Charakteristickým prejavom syndrómu je vznik
VAŠA DNA ANALÝZA Čo je Li- Fraumeni syndróm? Syndróm Li-Fraumeni je vrodené autozomálne dominantné ochorenie. Vzniká najčastejšie na podklade mutácie génu TP53. Charakteristickým prejavom syndrómu je vznik
VYKONÁVACIE NARIADENIE KOMISIE (EÚ) 2019/ zo 4. januára o povolení seleničitanu sodného, potiahnutého granulovaného selenič
 L 10/2 SK 14.1.2019 NARIADENIA VYKONÁVACIE NARIADENIE KOMISIE (EÚ) 2019/49 zo 4. januára 2019 o povolení seleničitanu sodného, potiahnutého granulovaného seleničitanu sodného a zinok-lselenometionínu ako
L 10/2 SK 14.1.2019 NARIADENIA VYKONÁVACIE NARIADENIE KOMISIE (EÚ) 2019/49 zo 4. januára 2019 o povolení seleničitanu sodného, potiahnutého granulovaného seleničitanu sodného a zinok-lselenometionínu ako
Ako vymeniť tlmiče prednej nápravy na Suzuki Swift 3
 Výmenu uskutočnite v nasledujúcom poradí: 1 Vymeňte zároveň oba tlmiče v rámci opravy vášho auta Suzuki Swift 3. 2 Zatiahnite páku ručnej brzdy. 3 Pod zadné kolesá umiestnite kliny. Uvoľnite upevňovacie
Výmenu uskutočnite v nasledujúcom poradí: 1 Vymeňte zároveň oba tlmiče v rámci opravy vášho auta Suzuki Swift 3. 2 Zatiahnite páku ručnej brzdy. 3 Pod zadné kolesá umiestnite kliny. Uvoľnite upevňovacie
Pedea, INN-Ibuprofen
 PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Pedea 5 mg/ml injekčný roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každý ml roztoku obsahuje 5 mg ibuprofenu. Každá ampulka s objemom
PRÍLOHA I SÚHRN CHARAKTERISTICKÝCH VLASTNOSTÍ LIEKU 1 1. NÁZOV LIEKU Pedea 5 mg/ml injekčný roztok 2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE Každý ml roztoku obsahuje 5 mg ibuprofenu. Každá ampulka s objemom
GENERÁLNY ŠTÁB
 GENERÁLNY ŠTÁB OZBROJENÝCH SÍL SLOVENSKEJ REPUBLIKY VOJENSKÁ ŠPECIFIKÁCIA Motorové palivá, oleje, mazivá, prevádzkové kvapaliny a špeciálne kvapaliny OLEJ LETECKÝ LO-12 Súvisiaci kód NATO O-147 Číslo MSU-26.4/L
GENERÁLNY ŠTÁB OZBROJENÝCH SÍL SLOVENSKEJ REPUBLIKY VOJENSKÁ ŠPECIFIKÁCIA Motorové palivá, oleje, mazivá, prevádzkové kvapaliny a špeciálne kvapaliny OLEJ LETECKÝ LO-12 Súvisiaci kód NATO O-147 Číslo MSU-26.4/L
Vnútroočné (fakické) šošovky ARTISAN na korekciu dioptrických chýb REF W; W; W; W Vnútroočné (torické fakické) šošovky ARTISAN
 Vnútroočné (fakické) šošovky ARTISAN na korekciu dioptrických chýb REF 202001W; 203001W; 204001W; 206001W Vnútroočné (torické fakické) šošovky ARTISAN na korekciu dioptrických chýb REF 110**1W; 120**1W;
Vnútroočné (fakické) šošovky ARTISAN na korekciu dioptrických chýb REF 202001W; 203001W; 204001W; 206001W Vnútroočné (torické fakické) šošovky ARTISAN na korekciu dioptrických chýb REF 110**1W; 120**1W;
Žiadosť o zaradenie dietetickej potraviny do zoznamu kategorizovaných dietetických potravín a úradné určenie ceny dietetickej potraviny Dietetická pot
 Žiadosť o zaradenie dietetickej potraviny do zoznamu kategorizovaných dietetických potravín a úradné určenie ceny dietetickej potraviny Dietetická potravina, ktorá svojou charakteristikou nepatrí do žiadnej
Žiadosť o zaradenie dietetickej potraviny do zoznamu kategorizovaných dietetických potravín a úradné určenie ceny dietetickej potraviny Dietetická potravina, ktorá svojou charakteristikou nepatrí do žiadnej
Prezentácia programu PowerPoint
 Inšpekcie Správnej farmakovigilančnej praxe Prehľad najčastejšie sa vyskytujúcich nedostatkov zistených pri inšpekciách SFP príprava, priebeh inšpekcie, kritériá pre posudzovanie závažnosti nálezov, CAPA,
Inšpekcie Správnej farmakovigilančnej praxe Prehľad najčastejšie sa vyskytujúcich nedostatkov zistených pri inšpekciách SFP príprava, priebeh inšpekcie, kritériá pre posudzovanie závažnosti nálezov, CAPA,
Naviten 600 mg PIL
 Písomná informácia pre používateľa NAVITEN 600 mg (eprosartani mesilas) filmom obalené tablety Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete užívať tento liek, pretože obsahuje pre
Písomná informácia pre používateľa NAVITEN 600 mg (eprosartani mesilas) filmom obalené tablety Pozorne si prečítajte celú písomnú informáciu predtým, ako začnete užívať tento liek, pretože obsahuje pre
Sandimmun - Art 30 - PI (capsules, OS and IV )
 PRÍLOHA I ZOZNAM NÁZVOV, FARMACEUTICKÝCH FORIEM, MNOŽSTVÁ ÚČINNÝCH LÁTOK V LIEKOCH, SPÔSOBY PODÁVANIA, DRŽITELIA ROZHODNUTIA O REGISTRÁCII V ČLENSKÝCH ŠTÁTOCH 1 Členský štát EÚ/EHP Držiteľ rozhodnutia
PRÍLOHA I ZOZNAM NÁZVOV, FARMACEUTICKÝCH FORIEM, MNOŽSTVÁ ÚČINNÝCH LÁTOK V LIEKOCH, SPÔSOBY PODÁVANIA, DRŽITELIA ROZHODNUTIA O REGISTRÁCII V ČLENSKÝCH ŠTÁTOCH 1 Členský štát EÚ/EHP Držiteľ rozhodnutia
